遼寧熱原檢測常見問題分析
來源:
發布時間:2025-10-11
PyroSHENTEK®熱原檢測試劑盒依據 ICH Q2 (R2)、《中國藥典》(如通則 9301)及歐洲藥典(EP 2.6.30)要求,完成了線性、范圍、定量限、準確度、精密度、耐用性等全維度性能驗證。線性方面,0.0125-1.0EU/mL范圍內擬合良好,R2≥0.98;準確度通過加標回收實驗驗證,不同樣品基質(如生物制品、化學制藥原料)的回收率均落在 50%-200% 區間;精密度表現優異,批內與批間 CV 均≤15%,且無論是 3 復孔還是 4 復孔檢測均能達標。此外,試劑盒使用中國藥典推薦的 MAT 特定標準品,可直接用于國內外申報,契合全球 “3R 原則” 監管導向—尤其適配《歐洲藥典》刪除家兔法、《美國藥典》鼓勵 MAT 替代等新法規趨勢,為企業應對不同地區的熱原檢測合規要求提供有力支持。
與傳統方法相比,MAT 法能更覆蓋各類熱原,保障產品安全性。遼寧熱原檢測常見問題分析
PBMC(外周血單個核細胞)的復雜制備流程嚴重制約熱原檢測效率。首先,血源獲取受獻血者數量、時間及采集血液政策限制,無法按需即時獲取;其次,需嚴格執行 EP2.6.30 規定的標志物檢測,增加前期準備時間;再進行采集血液、分離單核細胞、凍存等環節需全程無菌操作,步驟繁瑣且易引入污染風險。相比之下,單核細胞系可工業化培養,制備流程簡單可控,能快速提供合格細胞,避免因 PBMC 制備延誤熱原檢測進度,更適配批量樣品的高效質控。疫苗熱原檢測結果判定歐洲藥典已正式廢除家兔法熱原檢測,推薦單核細胞活化反應試驗(MAT)為合適的替代方案。
MAT 試劑盒熱原檢測配套細胞的質量控制,是保障檢測結果可靠的重要環節,需從功能、安全性、穩定性三方面建立體系。在功能鑒定上,按歐洲 MAT 法要求,需檢測細胞的 Toll 樣受體(TLR1-TLR9)表達情況—確保細胞能響應不同類型熱原(如 TLR4 響應 LPS、TLR2/6 響應脂磷壁酸);同時考察細胞倍增時間(確保活性穩定)、熱原反應性(對標準內毒素和非內毒素熱原的信號強度),確保細胞具備熱原識別與炎癥因子分泌能力。在安全性檢測上,需驗證細胞無菌(無細菌、真菌污染)、無支原體、無外源病毒因子(如 HIV、HBV)及分枝桿菌,避免外源污染影響檢測結果。在穩定性考察上,需監測不同代次細胞的熱原刺激敏感性,一般要求細胞使用代次不超過 20 代,代次過高會導致 TLR 表達下降、炎癥因子分泌減少,影響檢測靈敏度。湖州申科的配套細胞還額外通過 Western blot 驗證 TLR 受體表達量,并用不同非內毒素熱原配體刺激驗證響應性,形成全維度質量控制,確保細胞適配熱原檢測需求。
中國藥典與歐洲藥典對 MAT 熱原檢測的細胞類型及復孔數有明確要求,且存在細節差異。細胞類型上,兩者均認可人全血、PBMC(外周血單個核細胞,至少 4 個供體,歐洲藥典建議 8 個供體),中國藥典明確將單核細胞系納入,歐洲藥典則要求單核細胞系需做支原體污染檢測、細胞鑒別等;檢測方法均為 “熱原刺激細胞 + ELISA 檢測 IL-6/IL-1β/TNF-α”。復孔數方面,兩者均規定平行孔≥4、濃度點≥4,中國藥典額外要求標曲 r≥0.90,主要目的是通過多重復孔抵消 PBMC 的不穩定性,確保熱原檢測結果準確可靠。
湖州申科熱原檢測試劑盒中單核細胞系表面有多種Toll樣受體,可響應革蘭氏陽性菌、病毒等熱原。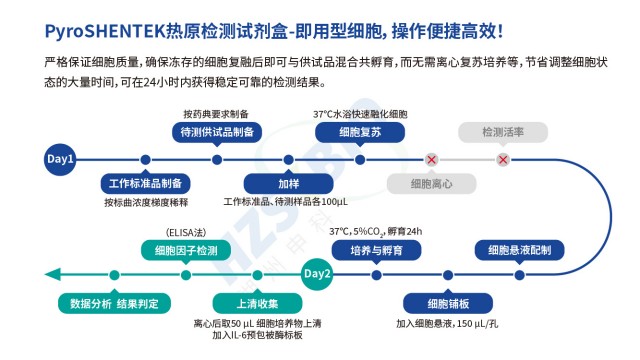
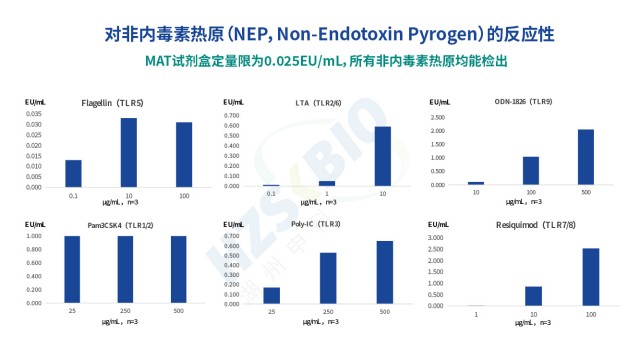
傳統細菌內毒素檢查法(BET)只能檢測革蘭氏陰性菌的 LPS,無法識別革蘭氏陽性菌 LTA、真菌酵母多糖、病毒鞭毛蛋白等非內毒素熱原,存在漏檢風險;同時,部分樣品(如脂質體、表面活性劑制劑)會因內毒素吸附導致低內毒素回收(LER),BET法難以準確定量。MAT 法通過單核細胞表面的多種 TLR 受體(TLR1-TLR10),可識別不同類型熱原:TLR4 識別 LPS、TLR2/TLR6 識別 LTA 與酵母多糖、TLR5 識別鞭毛蛋白、TLR3 識別病毒 dsRNA 等,實現 “全熱原覆蓋”。湖州申科生物熱原檢測試劑盒(MAT法)的驗證數據顯示,其對不同濃度非內毒素熱原均有響應:如 0.1-100μg/mL 鞭毛蛋白可檢測到 0.005-0.035EU/mL熱原活性,0.1-10μg/mL LTA 對應 0.1-0.7EU/mL 熱原活性,1-100μg/mL 雷西莫特(TLR7/8 配體)對應 0.5-3.0EU/mL 熱原活性。此外,MAT法檢測的是熱原的生物活性(而非單純 LPS 含量),可避免 LER 導致的假陰性,為CGT等高風險產品提供更有保障的熱原檢測方案。
憑借深厚的專業積累,湖州申科生物為行業提供可靠的熱原檢測解決方案。疫苗熱原檢測結果判定生物制品的高蛋白、螯合劑基質易對鱟試驗產生抑制,rCR與MAT聯合策略可消除干擾并控制熱原。遼寧熱原檢測常見問題分析
MAT法熱原檢測中,非內毒素熱原(NEP)對照品設為 “選做”,且試劑盒不默認配備,需結合檢測需求靈活使用,背后有明確的設置邏輯。首先,試劑盒開發階段已通過驗證(用多種 NEP 配體刺激細胞),證明其可檢出 NEP,后期實驗是否加入 NEP 對照,只需根據內部管理要求或專業人員建議確定,無需強制設置;若產品產線明確無 NEP 污染風險(如只使用革蘭氏陰性菌原料),可刪除 NEP 對照,簡化操作。其次,試劑盒不配備 NEP 對照品,是因不同用戶需求差異大 —— 部分用戶需檢測特定 NEP(如脂磷壁酸),部分需檢測廣譜 NEP,因此提供單獨購買選項,用戶可按需選擇,避免資源浪費。NEP 對照品的主要使用場景包括:一是方法驗證階段,用于確認試劑盒對 NEP 的響應性;二是產品工藝變更后,排查是否引入 NEP 污染;三是歐盟申報時,需證明方法可覆蓋 NEP,此時需加入 NEP 對照品并顯示陽性結果。若樣品檢測中 NEP 對照品陽性,而樣品檢測陰性,可排除 NEP 污染;若樣品陽性,則需進一步鑒定熱原類型。
遼寧熱原檢測常見問題分析
上一篇
上海高效熱原檢測操作步驟
下一篇:
甘肅qPCR法宿主細胞殘留DNA檢測
相關新聞
- 浙江合規性內毒素檢測低內毒素回收 2025-10-13
- 山西熱原檢測規范 2025-10-12
- 上海醫療器械熱原檢測MAT法 2025-10-12
- 江蘇合規性內毒素檢測凝膠法鱟試劑 2025-10-12
- 江蘇抗體藥物熱原檢測操作步驟 2025-10-12
- 浙江重組蛋白內毒素檢測合規申報 2025-10-12
- 廣東Human宿主細胞殘留DNA檢測生產企業 2025-10-12
- 北京熱原檢測風險評估 2025-10-12
- 成都單抗藥物用宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證 2025-10-12
- 遼寧熱原檢測結果判定 2025-10-12
推薦新聞
- 河北染色價位 2025-10-13
- 松江區名優實驗儀器工廠直銷 2025-10-13
- 體感誘發電位說明 2025-10-13
- 浙江家用缺血預適應訓練儀市場價 2025-10-13
- 遼寧合成高分子材料聚合輔助 2025-10-13
- 松江區試劑盒誠信合作 2025-10-13
- 山東中風缺血預適應訓練儀零售價 2025-10-13
- 淄博耐污涂層 2025-10-13
- 廣東蛋白質組學平臺 2025-10-13
- 蛋白質測定試劑盒 2025-10-13